世界のオンコロジー臨床試験市場規模/シェア/動向分析レポート:フェーズI、フェーズII、フェーズIII、フェーズIV

市場概要
世界のがん臨床試験市場規模は2022年に129.2億米ドルと推定され、2023年から2030年にかけて年平均成長率(CAGR)5.2%で成長すると予測されている。この市場を牽引している主な要因は、技術的進歩の増加、がん罹患率の上昇、個別化医療や細胞・遺伝子治療の改善などであり、これらはがんに似た疾患に対する新たな治療法開発のための新たなアプローチを開始している。さらに、製薬会社やバイオテクノロジー企業、非営利団体、CROからの腫瘍学臨床試験に対する資金提供の増加が、市場の成長をさらに後押ししており、市場シェアを大幅に拡大するための先進的な製品の開発が進んでいる。
世界市場を牽引しているのは、がん患者数の増加である。肺がんは、毎年180万人が診断されると推定され、世界中でがんに関連した死亡の主な原因として浮上すると予測されている。米国のがん患者数は2022年に190万人に達した。また、膵臓がんは予後が悪く、生存期間はわずか1〜3年である。この市場は、臨床試験参加に伴う文化的・社会的課題、臨床試験プロセスにおけるリクルートの障壁、科学的知識の欠如、統計やデータの誤用、試験プロトコルの複雑さなどの要因によって阻害されると予想される。
MooneyによるNational Center for Biomedical Imaging Clinical Trials Cooperative Group Programの説明によれば、National Center for Biomedical Imaging(NCI)は米国における全癌臨床試験の約50%に資金を提供している。しかし、COVID-19の大流行が腫瘍学の臨床試験を遅らせた。パンデミックの間、安全性への懸念や参加者の募集が困難であったため、多くの臨床試験が延期または遅延された。
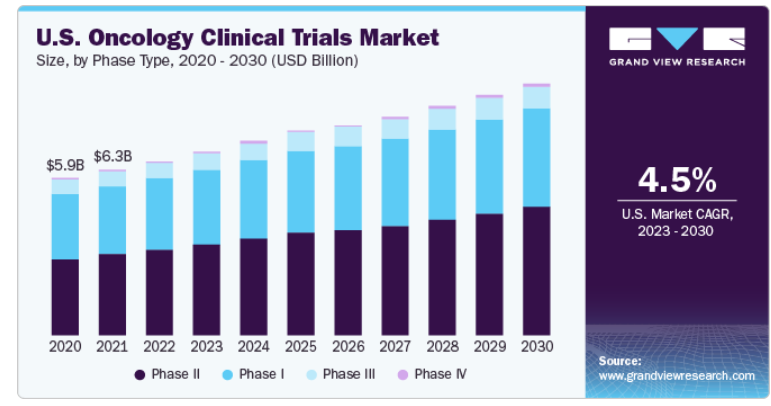
タイプ別に見ると、市場は第I相、第II相、第III相、第IV相に区分される。第I相臨床試験セグメントは、2022年に30.0%以上の最大の売上シェアを占めた。がん臨床試験業界における第I相臨床試験セグメントは、科学的、規制的、財政的、患者中心の要因によって推進される。臨床試験の第I相では、少人数の個人(20〜100人の健康なボランティア)が実験的な薬剤や治療法の試験を受ける。
第III相セグメントは、予測期間中最も速いCAGR 5.6%を記録すると推定される。第III相試験の推進要因としては、第III相試験のシェアが高いことが挙げられる。これは、第III相試験が最も費用がかかるが、多くの被験者を対象とするという事実に起因している。第III相試験では、登録および市販後公約のために長期安全性試験が実施される。例えば、2020年7月、HER2陽性進行乳癌患者に対する補助療法としての有用性と実行可能性を評価するため、ペルツズマブおよびトラスツズマブと併用するアルペリシブの第III相臨床試験がノバルティスAGによって開始された。
試験デザインに基づくと、介入試験セグメントは2022年に約87.6%の最大の売上シェアを占めた。がん臨床試験分野における介入試験デザインの推進要因は、主にこれらの疾患特有の課題にある。患者数が限られていることから、意味のある治療効果を検出する可能性を最大化するためには、試験を綿密にデザインする必要がある。
観察研究セグメントは、予測期間中に最も速いCAGR 6.1%を記録すると推定される。いくつかの推進要因により、観察試験デザインはがん臨床試験産業において重要な役割を果たしている。がん患者数が少ないため、従来のランダム化比較試験は困難であり、観察試験は治療の有効性と安全性を評価するためのより実行可能な選択肢となっている。
北米は市場を支配し、2022年には41.8%と最大の収益シェアを占め、予測期間中もその優位性を維持すると予想される。この地域にはさまざまな有利な償還政策があり、主要な市場プレーヤーが存在するため、投資や革新的な製品の開発につながっている。また、米国FDAは、がん治療薬の承認プロセスを迅速化している。例えば、米国政府説明責任局によると、保健社会福祉省(HHS)傘下の機関である国立衛生研究所(NIH)は、生物医学研究開発(R&D)の最も重要な公的資金提供者である。
2017年から2021年の会計年度において、NIHは基礎研究に970億米ドル、臨床試験と関連事業に280億米ドルという驚異的な予算を割り当てている。一方、アジア太平洋地域は予測期間中、CAGR 7.1%と最も速い成長が見込まれている。これは、同地域に食品医薬品局(FDA)、医薬品医療機器局(TGA)、欧州医薬品庁(EMA)の認可を受けた施設が多数あるためである。さらに、この地域では患者数が多く、臨床試験の実施コストが低いことも、この地域の市場をさらに後押ししている。
主要企業・市場シェア
がん領域の臨床試験業界は競争が激しく、多数のメーカーが市場シェアの大半を占めている。相の上市、承認、戦略的買収、提携、技術革新は、市場参加者が世界的なリーチを維持・拡大するために用いる重要な事業戦略のほんの一部に過ぎない。
主なオンコロジー臨床試験企業
アストラゼネカ
メルク社
IQVIA社
ギリアド・サイエンシズ
F. ホフマン・ラ・ロシュ社
パレクセル・インターナショナル株式会社
PRAヘルスサイエンス
シネオス・ヘルス
メドスペース
ノボテック
ピボタル
本レポートでは、世界、地域、国レベルでの収益成長を予測し、2018年から2030年までの各サブセグメントにおける最新の業界動向の分析を提供しています。この調査について、Grand View Research社は世界のがん臨床試験市場レポートをフェーズタイプ、試験デザイン、地域に基づいてセグメント化しています:
フェーズタイプの展望(売上高、百万米ドル、2018年~2030年)
フェーズI
フェーズII
フェーズIII
フェーズIV
試験デザインの展望(収益、百万米ドル、2018年~2030年)
介入研究
観察研究
拡張アクセス試験
地域別展望(売上高、百万米ドル、2018年~2030年)
北米
米国
カナダ
欧州
英国
ドイツ
フランス
イタリア
スペイン
デンマーク
スウェーデン
ノルウェー
アジア太平洋
中国
日本
インド
オーストラリア
タイ
韓国
ラテンアメリカ
ブラジル
メキシコ
アルゼンチン
中東・アフリカ
南アフリカ
サウジアラビア
UAE
クウェート
【目次】
第1章 方法論と範囲
1.1 市場セグメンテーション
1.2 調査方法
1.3 情報収集
1.3.1 購入データベース
1.3.2 GVRの社内データベース
1.3.3 二次情報源
1.3.4 一次調査
1.4 情報またはデータ分析
1.4.1 データ分析モデル
1.5 市場策定と検証
1.6 モデルの詳細
1.6.1 商品フロー分析
1.6.1.1 商品フロー分析(モデル1)
1.6.1.1.1 アプローチ1:商品フローアプローチ
1.7 二次資料リスト
1.8 略語一覧
1.9 目的
1.9.1 目的1
1.9.2 目的2
1.9.3 目的3
第2章 エグゼクティブ・サマリー
2.1 市場展望
2.1.1 地域別の洞察
2.1.2 競争環境
2.2 市場スナップショット
2.3 セグメント別スナップショット
2.4 セグメント別スナップショット
2.5 競合の状況
第3章 がん臨床試験市場の変数と動向
3.1 市場ダイナミクス
3.1.1 市場ドライバーの影響分析
3.1.1.1 癌の有病率の増加
3.1.1.2 研究活動を行うCRO数の増加
3.1.2 市場抑制インパクト分析
3.1.2.1 がん臨床試験に伴う高コスト
3.1.3 市場機会インパクト分析
3.1.3.1 技術の進歩
3.1.4 市場課題インパクト分析
3.1.4.1 臨床試験の患者登録に関する厳しい規制
3.2 業界分析ツール
3.2.1 ポーター分析
3.2.2 マクロ経済分析
第4章 がん臨床試験市場 フェーズタイプ分析
4.1 タイプ別動向分析と市場シェア、2022年・2030年
4.2 オンコロジー臨床試験市場のフェーズ別推定・予測(百万米ドル)
4.3 タイプ別市場規模・予測およびトレンド分析、2018年〜2030年
4.3.1 フェーズI
4.3.1.1 フェーズI市場、2018年〜2030年(USD Million)
4.3.2 フェーズII
4.3.2.1 フェーズII市場、2018年~2030年(百万米ドル)
4.3.3 フェーズIII
4.3.3.1 フェーズIII市場、2018年~2030年(百万米ドル)
4.3.4 第Ⅳ相
4.3.4.1 第IV相市場、2018年~2030年(百万米ドル)
第5章 がん領域の臨床試験市場 試験デザイン分析
5.1 試験デザインの動向分析と市場シェア、2022年・2030年
5.2 オンコロジー臨床試験市場の推定と予測、試験デザイン別(USD Million)
5.3 試験デザイン別市場規模・予測および動向分析、2018年〜2030年
5.3.1 インターベンション
5.3.1.1 インターベンション市場、2018年〜2030年(百万米ドル)
5.3.2 観察
5.3.2.1 観察市場、2018年~2030年(百万米ドル)
5.3.3 拡張アクセス試験
5.3.3.1 拡大アクセス市場、2018年~2030年(USD Million)
第6章 がん領域の臨床試験市場 地域別推定と動向分析
6.1 がん領域の臨床試験市場 地域別展望
6.2 北米
6.2.1 北米のがん臨床試験市場の推計と予測、2018年〜2030年(百万米ドル)
6.2.2 米国
6.2.2.1 主要国のダイナミクス
6.2.2.2 米国のがん臨床試験市場の推計と予測、2018年~2030年(百万米ドル)
6.2.3 カナダ
6.2.3.1 主要国の動向
6.2.3.2 カナダのがん臨床試験市場の推計と予測、2018年~2030年(百万米ドル)
6.3 欧州
6.3.1.1 欧州のがん臨床試験市場の推計と予測、2018年~2030年(百万米ドル)
6.3.2 英国
6.3.2.1 主要国のダイナミクス
6.3.2.2 英国のがん臨床試験市場の推計と予測、2018年~2030年(百万米ドル)
6.3.3 ドイツ
6.3.3.1 主要国の動向
6.3.3.2 ドイツのがん臨床試験市場の推計と予測、2018年~2030年(百万米ドル)
6.3.4 フランス
6.3.4.1 主要国の動向
6.3.4.2 フランスのがん臨床試験市場の推計と予測、2018年~2030年(百万米ドル)
6.3.5 イタリア
6.3.5.1 主要国の動向
6.3.5.2 イタリアのがん臨床試験市場の推計と予測、2018年~2030年(百万米ドル)
6.3.6 スペイン
6.3.6.1 主要国の動向
6.3.6.2 スペインのがん臨床試験市場の推計と予測、2018年~2030年(百万米ドル)
6.3.7 スウェーデン
6.3.7.1 主要国の動向
6.3.7.2 スウェーデンのがん臨床試験市場の推計と予測、2018年~2030年(百万米ドル)
6.3.8 デンマーク
6.3.8.1 主要国の動向
6.3.8.2 デンマークのがん臨床試験市場の推計と予測、2018年~2030年(百万米ドル)
6.3.9 ノルウェー
6.3.9.1 主要国の市場動向
6.3.9.2 ノルウェーのがん臨床試験市場の推定と予測、2018年~2030年(百万米ドル)
6.4 アジア太平洋
6.4.1.1 アジア太平洋地域のがん臨床試験市場の推計と予測、2018年~2030年(百万米ドル)
6.4.2 日本
6.4.2.1 主要国のダイナミクス
6.4.2.2 日本のがん臨床試験市場の推計と予測、2018年~2030年(百万米ドル)
6.4.3 中国
6.4.3.1 主要国の動向
6.4.3.2 中国のがん臨床試験市場の推計と予測、2018年~2030年(百万米ドル)
6.4.4 インド
6.4.4.1 主要国の動向
6.4.4.2 インドのがん臨床試験市場の推計と予測、2018年~2030年(百万米ドル)
6.4.5 オーストラリア
6.4.5.1 主要国の動向
6.4.5.2 オーストラリアのがん臨床試験市場の推計と予測、2018年~2030年(百万米ドル)
6.4.6 韓国
6.4.6.1 主要国の動向
6.4.6.2 韓国のがん臨床試験市場の推計と予測、2018年~2030年(百万米ドル)
6.4.7 タイ
6.4.7.1 主要国の動向
6.4.7.2 タイのがん臨床試験市場の推計と予測、2018年~2030年(百万米ドル)
6.5 ラテンアメリカ
6.5.1.1 中南米のがん臨床試験市場の推計と予測、2018年~2030年(USD Million)
6.5.2 ブラジル
6.5.2.1 主要国のダイナミクス
6.5.2.2 ブラジルのがん臨床試験市場の推定と予測、2018年~2030年(百万米ドル)
6.5.3 メキシコ
6.5.3.1 主要国の動向
6.5.3.2 メキシコのがん臨床試験市場の推計と予測、2018年~2030年(百万米ドル)
6.5.4 アルゼンチン
6.5.4.1 主要国の動向
6.5.4.2 アルゼンチンのがん臨床試験市場の推計と予測、2018年~2030年(百万米ドル)
6.6 中東・アフリカ
6.6.1.1 中東・アフリカのがん臨床試験市場の推計と予測、2018年~2030年(百万米ドル)
6.6.2 南アフリカ
6.6.2.1 主要国のダイナミクス
6.6.2.2 南アフリカのがん臨床試験市場の推計と予測、2018年~2030年(百万米ドル)
6.6.3 サウジアラビア
6.6.3.1 主要国の市場動向
6.6.3.2 サウジアラビアのがん臨床試験市場の推計と予測、2018年~2030年(百万米ドル)
6.6.4 アラブ首長国連邦
6.6.4.1 主要国の市場動向
6.6.4.2 アラブ首長国連邦のがん臨床試験市場の推計と予測、2018年~2030年(百万米ドル)
6.6.5 クウェート
6.6.5.1 主要国の動向
6.6.5.2 クウェートのがん臨床試験市場の推定と予測、2018年~2030年(百万米ドル)
…
【本レポートのお問い合わせ先】
www.marketreport.jp/contact
レポートコード:GVR-4-68039-139-7