世界のアデノ随伴ウイルス遺伝子治療市場~2034:地域別(北米、アジア太平洋、ヨーロッパ、中南米、中東・アフリカ)分析

市場規模
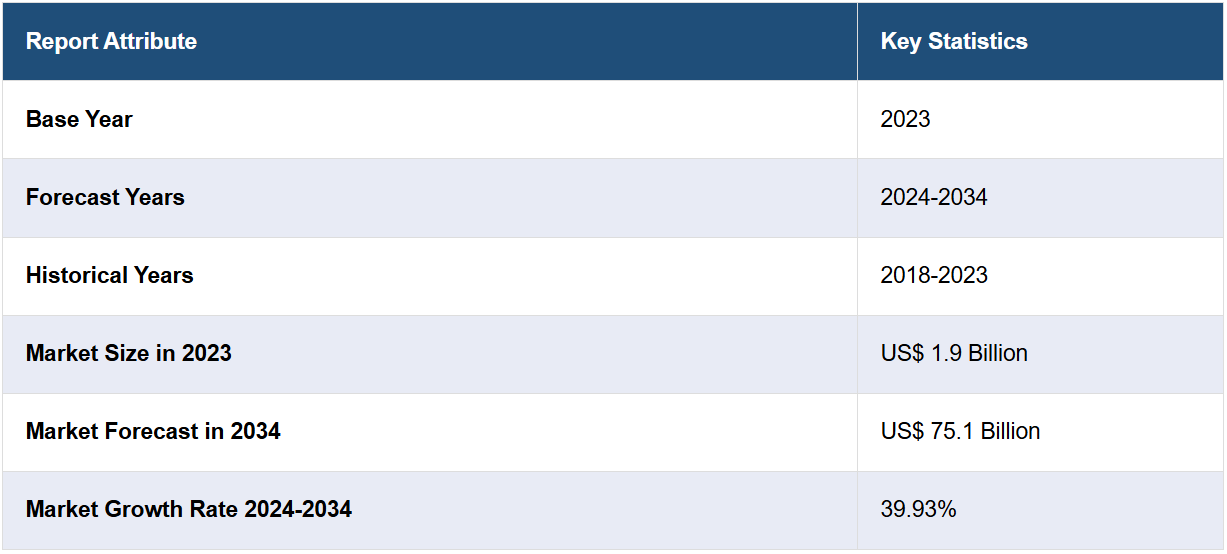
7つの主要なアデノ随伴ウイルス遺伝子治療市場は、2023年に19億米ドルの価値に達しました。IMARC Groupは、今後、7MMが2034年までに751億米ドルに達し、2024年から2034年の年間平均成長率(CAGR)は39.93%になると予測しています。
アデノ随伴ウイルス遺伝子治療市場は、IMARCの最新レポート「アデノ随伴ウイルス遺伝子治療市場: 疫学、業界動向、シェア、規模、成長、機会、予測 2024年~2034年」と題された。 アデノ随伴ウイルス(AAV)遺伝子治療は、アデノ随伴ウイルスを利用して遺伝物質を体内の細胞に送達する遺伝子治療の一種である。AAVは、分裂細胞にも非分裂細胞にも感染する小型の非病原性ウイルスであり、遺伝子治療に有用なベクターとなる。ウイルス遺伝子を一切含まない、目的のDNA配列を含む組換えAAV粒子を生成する能力は、最も活発に研究されている遺伝子治療ベクターのひとつです。現在、2種類の組換えAAV(rAAV)が使用されています。自己相補性AAV(scAAV)と一本鎖AAV(ssAAV)です。組換えアデノ随伴ウイルス遺伝子治療には、遺伝子サイレンシング、遺伝子置換、遺伝子付加、遺伝子編集があります。AAVには、12種類の天然の血清型(AAV血清型1 [AAV-1] から AAV-12] および100以上の変異型が存在し、それぞれが独特のアミノ酸配列、特にカプシドタンパク質の超可変領域内に特有のアミノ酸配列を有しているため、遺伝子導入特性もわずかに異なります。また、AAVは比較的容易に生産および精製できるため、費用対効果の高い遺伝子治療オプションとなります。AAV遺伝子治療には、標的送達、長期有効性、低毒性、1回限りの治療の可能性など、いくつかの利点があります。
遺伝性疾患、特定のタイプの癌、多数のウイルス感染症など、幅広い疾患の治療に有効なAAV遺伝子治療の能力が向上していることが、世界的なアデノ随伴ウイルス遺伝子治療市場の主な推進要因となっています。これに加えて、臨床応用に有益ないくつかのユニークな特徴、すなわち低免疫原性、幅広い指向性、生産の容易性などにより、AAVベクターの人気が高まっていることも、市場の見通しをさらに明るいものにしています。AAVは非病原性であり、宿主染色体に組み込まれることはまれで、導入遺伝子を長期間発現させることができます。さらに、高収率の生産細胞株を可能にするAAV遺伝子治療の研究開発活動には、さまざまな主要企業が大規模な投資を行っています。これにより、より高品質で柔軟性のあるウイルスベクター生産を低コストで実現できるようになります。これが、さらなる成長を促す重要な要因となっています。さらに、患者の特定の遺伝子変異に容易に適合させることができるため、より効果的な治療につながるAAV遺伝子治療の個別化治療への利用が拡大していることも、世界市場を後押ししています。さらに、導入遺伝子カセットの最適化によるAAVの伝達効率の改善や、ベクターの指向性を高めるためのキャプシド工学の利用など、バイオテクノロジーおよび遺伝学分野における継続的な進歩が、今後数年間で世界のアデノ随伴ウイルス遺伝子治療市場を牽引することが期待されています。
IMARC Groupの最新レポートは、米国、EU5(ドイツ、スペイン、イタリア、フランス、英国)、日本におけるアデノ随伴ウイルス遺伝子治療市場を徹底的に分析しています。これには、治療慣行、市場内、パイプラインの薬剤、個々の治療法のシェア、7つの主要市場にわたる市場実績、主要企業およびその薬剤の市場実績などが含まれます。また、このレポートでは、7つの主要市場における現在の患者数と将来の患者数も提供しています。このレポートによると、アデノ随伴ウイルス遺伝子治療の患者数が最も多いのは米国であり、また、その治療の市場規模も最大です。さらに、現在の治療方法/アルゴリズム、市場の推進要因、課題、機会、償還シナリオ、未充足の医療ニーズなどもレポートに記載されています。このレポートは、アデノ随伴ウイルス遺伝子治療市場に何らかの利害関係を有する、または何らかの形で市場参入を計画しているメーカー、投資家、経営戦略担当者、研究者、コンサルタントなどすべての方にとって必読のレポートです。
調査期間
基準年:2023年
歴史的期間:2018年~2023年
市場予測:2024年~2034年
対象国
米国
ドイツ
フランス
英国
イタリア
スペイン
日本
各国における分析内容
過去、現在、将来の疫学シナリオ
過去、現在、将来のアデノ随伴ウイルス遺伝子治療市場の実績
市場における各種治療カテゴリーの過去、現在、将来の実績
アデノ随伴ウイルス遺伝子治療市場における各種薬剤の売上
市場における償還シナリオ
市場および開発中の薬剤
競合状況
このレポートでは、現在市場に出回っているアデノ随伴ウイルス遺伝子治療薬と後期開発段階にある薬剤候補の詳細な分析も提供しています。
市場に出回っている薬剤
薬剤概要
作用機序
規制状況
臨床試験結果
薬剤の普及と市場実績
後期開発段階にある薬剤
薬剤概要
作用機序
規制状況
臨床試験結果
薬剤の普及と市場実績
【目次】
1 序文
2 範囲と方法論
2.1 本調査の目的
2.2 利害関係者
2.3 データソース
2.3.1 一次ソース
2.3.2 二次ソース
2.4 市場推定
2.4.1 ボトムアップアプローチ
2.4.2 トップダウンアプローチ
2.5 予測方法論
3 エグゼクティブサマリー
4 アデノ随伴ウイルス遺伝子治療 – イントロダクション
4.1 概要
4.2 規制プロセス
4.3 疫学(2018年~2023年)および予測(2024年~2034年
4.4 市場概要(2018年~2023年)および予測(2024年~2034年
4.5 競合情報
5 アデノ随伴ウイルス遺伝子治療 – 疾患概要
5.1 はじめに
5.2 症状と診断
5.3 病態生理学
5.4 原因とリスク要因
5.5 治療
6 患者の経過
7 アデノ随伴ウイルス遺伝子治療 – 疫学と患者数
7.1 疫学 – 主な洞察
7.2 疫学シナリオ – トップ7市場
7.2.1 疫学シナリオ(2018年~2023年
7.2.2 疫学予測(2024年~2034年
7.2.3 年齢別疫学(2018年~2034年
7.2.4 性別疫学(2018年~2034年
7.2.5 タイプ別疫学(2018年~2034年)
7.2.6 診断された症例(2018年~2034年)
7.2.7 患者数/治療された症例(2018年~2034年)
7.3 疫学シナリオ – 米国
7.3.1 疫学シナリオ(2018年~2023年)
7.3.2 疫学予測(2024年~2034年)
7.3.3 年齢別疫学(2018年~2034年)
7.3.4 性別疫学(2018年~2034年)
7.3.5 タイプ別疫学(2018年~2034年)
7.3.6 診断された症例(2018年~2034年)
7.3.7 患者数/治療された症例(2018年~2034年)
7.4 疫学シナリオ – ドイツ
7.4.1 疫学シナリオ(2018年~2023年)
7.4.2 疫学予測(2024年~2034年)
7.4.3 年齢別疫学(2018年~2034年)
7.4.4 性別疫学(2018年~2034年)
7.4.5 タイプ別疫学(2018年~2034年)
7.4.6 診断された症例(2018年~2034年)
7.4.7 患者数/治療例(2018年~2034年)
7.5 疫学シナリオ – フランス
7.5.1 疫学シナリオ(2018年~2023年)
7.5.2 疫学予測(2024年~2034年)
7.5.3 年齢別疫学(2018年~2034年)
7.5.4 性別による疫学(2018年~2034年)
7.5.5 タイプ別による疫学(2018年~2034年)
7.5.6 診断された症例(2018年~2034年)
7.5.7 患者数/治療された症例(2018年~2034年)
7.6 英国の疫学シナリオ
7.6.1 疫学シナリオ(2018年~2023年)
7.6.2 疫学予測(2024年~2034年)
7.6.3 年齢別疫学(2018年~2034年)
7.6.4 性別疫学(2018年~2034年)
7.6.5 タイプ別疫学(2018年~2034年)
7.6.6 診断された症例(2018年~2034年)
7.6.7 患者数/治療された症例(2018年~2034年)
7.7 疫学シナリオ – イタリア
7.7.1 疫学シナリオ(2018年~2023年)
7.7.2 疫学予測(2024年~2034年)
7.7.3 年齢別疫学(2018年~2034年)
7.7.4 性別疫学(2018年~2034年)
7.7.5 タイプ別疫学(2018年~2034年)
7.7.6 診断された症例(2018年~2034年)
7.7.7 患者数/治療された症例(2018年~2034年)
7.8 疫学シナリオ – スペイン
7.8.1 疫学シナリオ(2018年~2023年)
7.8.2 疫学予測(2024年~2034年)
7.8.3 年齢別感染症(2018年~2034年)
7.8.4 性別感染症(2018年~2034年)
7.8.5 タイプ別感染症(2018年~2034年)
7.8.6 診断された症例(2018年~2034年)
7.8.7 患者数/治療例数(2018年~2034年)
7.9 日本の疫学シナリオ
7.9.1 疫学シナリオ(2018年~2023年)
7.9.2 疫学予測(2024年~2034年)
7.9.3 年齢別疫学(2018年~2034年)
7.9.4 性別による疫学(2018年~2034年)
7.9.5 タイプ別による疫学(2018年~2034年)
7.9.6 診断された症例(2018年~2034年)
7.9.7 患者数/治療された症例(2018年~2034年)
8 アデノ随伴ウイルス遺伝子治療 – 治療アルゴリズム、ガイドライン、および医療行為
8.1 ガイドライン、管理、および治療
8.2 治療アルゴリズム
9 アデノ随伴ウイルス遺伝子治療 – 未充足ニーズ
10 アデノ随伴ウイルス遺伝子治療 – 治療の主要評価項目
11 アデノ随伴ウイルス遺伝子治療 – 上市製品
11.1 トップ7市場におけるアデノ随伴ウイルス遺伝子治療の上市済み薬剤の一覧
11.1.1 Luxturna (voretigene neparvovec-rzyl) – Spark Therapeutics, Inc.
11.1.1.1 薬剤の概要
11.1.1.2 作用機序
11.1.1.3 臨床試験結果
11.1.1.4 安全性および有効性
11.1.1.5 規制当局による審査状況
11.1.2 Zolgensma (onasemnogene abeparvovec) – Novartis Gene Therapies, Inc.
11.1.2.1 薬剤概要
11.1.2.2 作用機序
11.1.2.3 臨床試験結果
11.1.2.4 安全性および有効性
11.1.2.5 規制上のステータス
11.1.3 Glybera (alipogene tiparvovec) – uniQure
11.1.3.1 薬剤概要
11.1.3.2 作用機序
11.1.3.3 臨床試験結果
11.1.3.4 安全性および有効性
11.1.3.5 規制上のステータス
…
【お問い合わせ・ご購入サイト】
資料コード:SR112025A6765
