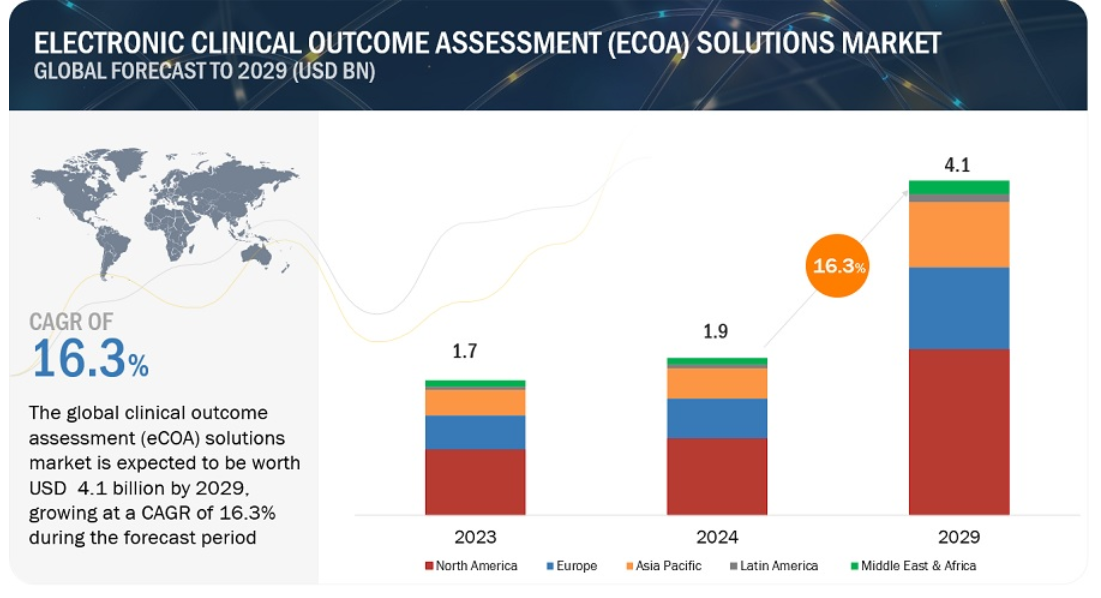
電子臨床アウトカム評価/eCOAソリューションの世界市場は2029年までにCAGR 16.3%で成長する見通し

電子臨床転帰評価ソリューションの世界市場は、収益ベースで2024年に19億ドル規模と推定され、2024年から2029年までの年平均成長率は16.3%で、2029年には41億ドルに達する見通しである。この新しい調査研究は、市場の業界動向分析で構成されています。この新しい調査研究は、業界動向、価格分析、特許分析、会議とウェビナー資料、主要関係者、市場における購買行動で構成されています。
市場動向
推進要因:臨床研究に関連する運用コストと規制要件の上昇
臨床試験は高額であり、1つのフェーズで数百万ドルに達すると見積もられている。患者募集、施設管理、データ収集などの要因が、この膨大なコストに大きく寄与している。eCOAソリューション市場を牽引する原動力として、臨床試験に関する運用コストの急増と規制要件の強化が際立っている。臨床研究は複雑さが大幅に増しており、より複雑な方法論、広範なデータ収集、進化する規制基準の厳格な遵守が必要となっている。このような複雑さは、施設モニタリング、データ管理、参加者募集などの側面をカバーする運営費の上昇につながる。規制当局は、確実なエビデンス作成の必要性を認識しているため、包括的で標準化されたデータ収集方法を必要としている。このような厳しい規制ガイドラインを遵守するためには、データ収集、検証、報告プロセスを合理化し、効率を高めるように設計されたeCOAソリューションのような高度な技術が必要である。
コンプライアンスの負担が増大し続ける中、製薬、バイオテクノロジー、医療機器の各企業は、業務上の課題を軽減し、コストを削減し、規制コンプライアンスを確保するために、eCOAソリューションを採用するケースが増えている。このように、運用コストと規制要件の上昇は、eCOAソリューションの採用を増加させ、臨床研究分野で必要なツールとして位置づけている。
阻害要因:エンドユーザーのeCOAソリューションに対する認識不足
エンドユーザーのeCOAソリューションに対する認識不足は、市場が直面する主要な障害である。これは、eCOA技術の存在、利点、機能性に関する医療従事者、患者、その他の利害関係者の知識のギャップを助長し、eCOAの広範な普及に大きな障害となっている。さらに、従来型のアプローチから電子ソリューションへの移行には、文化的な転換と意識の向上が必要である。医療提供者、臨床医、患者は、データ精度の向上、リアルタイムのモニタリング、患者エンゲージメントの改善など、eCOAソリューションが提供する利点を十分に認識していない可能性がある。このような認識不足は、新しい技術を取り入れることへの抵抗につながり、従来の評価方法への依存を永続させる可能性がある。
この制約には、eCOAソリューションに関する認識を高めることを目的とした、的を絞った教育的イニシアチブによって対処することができる。医療従事者向けのトレーニング・プログラム、患者向けの情報提供キャンペーン、業界内の協力的な取り組みなどが、認知度ギャップの解消に貢献できる。
機会: 新興国における臨床試験数の増加によるeCOA導入の急増
新興国は、大規模で多様な患者集団、費用対効果、より円滑な臨床試験プロセスを促進する規制環境の進化など、いくつかの要因から臨床試験活動の急速な成長を目の当たりにしている。これらの国々がグローバルな臨床研究の主要なプレーヤーとなるにつれ、eCOAソリューションのような高度で効率的なデータ収集ツールに対する需要が高まっている。これらの新興国は、遺伝的多様性のスペクトルが広く、特定の疾患の有病率が高いことが多いため、臨床研究により代表的なサンプルを提供することができます。製薬企業やバイオテクノロジー企業は、世界の人口動態をよりよく反映した集団で臨床試験を実施し、試験結果の一般化可能性を高めることの意義を認識している。新興国における臨床試験活動の継続的な成長は、eCOAソリューション市場に大きな機会をもたらす。この傾向はイノベーションの道筋を提供し、世界の臨床研究業界におけるデータの質を向上させる。この機会を効果的に活用することで、新興国全体でeCOAソリューションの採用を促進することができる。
課題:進化する規制環境とコンプライアンス要件
臨床試験や医療データを管理する規制環境は地域によって異なり、国ごとに多様な基準やコンプライアンスの枠組みが導入されています。この多様性は、eCOAソリューション・プロバイダーにとって、自社のプラットフォームが進化する規制の期待に確実に沿うように努力する上で、大きな課題となる。さらに、eCOAソリューション市場は、規制方針と要件の頻繁な更新を特徴とする環境で運営されている。米国食品医薬品局(FDA)や欧州医薬品庁(EMA)などの規制機関は、臨床試験における電子データ収集に関するガイドラインや期待事項を定期的に改訂している。ソリューションプロバイダーがリスクを軽減し、コンプライアンス基準を維持するためには、これらの変更を先取りし、eCOAプラットフォームに迅速に組み込むことが不可欠です。この課題は、臨床試験とヘルスケア研究のグローバルな性質によってさらに増幅されます。多施設臨床試験はしばしば異なる大陸にまたがり、それぞれが規制の枠組みによって管理されているからです。
電子臨床アウトカム評価(eCOA)ソリューション市場のエコシステムは、これらのソリューションをエンドユーザーに提供する責任を負う事業体で構成される。
eCOAソリューション市場は、様々な展開モデルを通じてエンドユーザーにこれらのソリューションを提供する事業体から構成される。eCOAソリューション市場全体のエコシステム市場マップは、この市場に存在する要素で構成され、これらの要素を関係機関のデモンストレーションとともに定義しています。この市場のエコシステムは、データセンタープロバイダー、ネットワーク/接続プロバイダー、クラウド専門プラットフォームプロバイダー、ハードウェアおよびサポートインフラストラクチャープロバイダーなど、さまざまなベンダーで構成されている。
ソフトウェアセグメントは、電子臨床転帰評価ソリューション産業2024年から2029年にかけて最も高いCAGRで成長すると予想される。
コンポーネントに基づいて、電子臨床アウトカム評価ソリューション市場は、ソフトウェア、サービス、ウェアラブル、モバイルデバイス、およびその他のデバイスにセグメント化されます。このうち、ソフトウェアサブセグメントが2023年のeCOAソリューション市場を支配しているが、これはいくつかの重要な要因によるものである。ソフトウェアはeCOAシステムの中核インフラを形成し、効率的なデータ収集、管理、分析を促進する技術的バックボーンとして機能する。この極めて重要な役割により、ソフトウェアはeCOAソリューションのシームレスな機能にとって不可欠なコンポーネントとして位置づけられている。ソフトウェアは、電子患者報告アウトカム(ePRO)機能、データ統合、リアルタイムモニタリングなどの多様な機能を包含し、研究者や医療専門家に包括的なツール群を提供するため、eCOAソリューション市場を支配している。
電子患者報告アウトカム(EPRO)セグメントは、2023年に電子臨床アウトカム評価ソリューション産業で最大のシェアを占めた。
製品別では、電子臨床アウトカム評価ソリューション市場は、電子患者報告アウトカム(ePRO)、電子臨床医報告アウトカム(eCLINRO)、電子観察者報告アウトカム(eOBSRO)、電子パフォーマンス報告アウトカム(ePERFO)に区分される。2023年には、電子患者報告アウトカム(EPRO)分野が最大の市場シェアを占めた。EPROは、患者が自分の症状、健康状態、治療に関連する転帰をリアルタイムで積極的に報告するもので、臨床データ収集に対する患者中心のアプローチを促進する。この方法は、患者の視点を総合的に理解できるだけでなく、データの正確性と豊かさを高め、より強固な臨床試験とヘルスケア研究に貢献する。さらに、規制機関や医療関係者は、治療の有効性と安全性の評価に患者の体験を取り入れることの重要性を認めており、そのため電子患者報告アウトカムがこのセグメントを支配している。
2023年の電子臨床アウトカム評価ソリューション業界では、製薬・バイオテクノロジー企業が最大のシェアを占めている。
エンドユーザーに基づいて、電子臨床アウトカム評価ソリューション市場は製薬&バイオテクノロジー企業、契約研究機関(CRO)、医療技術企業、政府機関、研究センター&学術機関、病院&医療プロバイダー、コンサルティングサービス企業に区分される。製薬・バイオテクノロジー企業セグメントは、医薬品開発および臨床研究において中心的な役割を担っていることから、2023年の電子臨床アウトカム評価(eCOA)ソリューション市場で最大のシェアを占めている。これらの企業は、効率的で厳格な臨床試験を実施するためにeCOAソリューションに大きく依存しており、規制当局の承認を得て新しい治療法を市場に投入するために不可欠である。さらに、これらの製薬およびバイオテクノロジーが満たさなければならない厳しい規制要件が存在するため、堅牢なデータ収集方法に対する需要が高まっている。eCOAソリューションはこれらの規制基準を満たすのに役立つため、多くの製薬企業やバイオテクノロジー企業がeCOAソリューションを採用している。
地域別に見ると、電子臨床転帰評価(eCOA)ソリューション市場は、北米、欧州、アジア太平洋地域、中南米、中東・アフリカに区分される。北米は、2023年の電子臨床アウトカム評価(eCOA)ソリューション市場で最大のシェアを占めている。これは、医薬品開発や臨床研究をリードする多数の製薬企業やバイオテクノロジー企業が存在し、eCOAソリューションのような高度な臨床データ収集ツールに対する大きな需要を生み出しているためである。さらに北米は、先進医療技術の導入を促進する有利な規制環境の恩恵を受けている。同地域の規制機関は、eCOAソリューションが提供するデータの正確性と患者の安全性を優先している。
主要企業
電子臨床アウトカム評価(eCOA)ソリューション市場の主要企業には、IQVIA(米国)、Medidata(米国)、ICON Plc(アイルランド)、Signant Health(米国)、Clario(米国)、Oracle Corporation(米国)、Medable Inc.(米国)、Merative(米国)、Parexel International (MA) Corporation(米国)、Climedo Health GmbH(ドイツ)、Healthentia(ベルギー)、Veeva Systems(米国)、assisTek(米国)、Curebase Inc. (米国)、Castor(米国)、EvidentIQ Group GmbH(ドイツ)、YPrime, LLC(米国)、Clinical Ink(米国)、Clinion(米国)、Kayentis(フランス)、TransPerfect(米国)、ObvioHealth USA, Inc.(米国)、WCG Clinical(ドイツ)、ClinCapture(米国)、Cloudbyz(米国)。
この調査では、電子臨床転帰評価ソリューション市場を分類し、以下の各サブマーケットにおける収益予測と動向分析を行っています:
コンポーネント別
ソフトウェア
サービス
ウェアラブル、モバイルデバイス、その他のデバイス
BYOD(Bring Your Own Device)モデル
プロビジョンド・デバイス・モデル
ハイブリッド・モデル
製品タイプ別
電子患者報告アウトカム(ePRO)
臨床医が報告する電子アウトカム(eCLINRO)
電子観察者報告アウトカム(eOBSRO)
電子パフォーマンス報告アウトカム(ePERFO)
導入モデル別
オンプレミスモデル
ウェブホスト&クラウドベースモデル
ハイブリッドモデル
応用分野別
臨床試験
腫瘍学
感染症
神経学
代謝性疾患
心血管疾患
免疫学
希少疾患・遺伝性疾患
精神疾患
その他の治療領域
観察研究&リアルワールドエビデンス(RWE)作成
患者管理および登録
その他のアプリケーション
エンドユーザー別
製薬・バイオテクノロジー企業
医薬品開発業務受託機関(CRO)
医療技術企業
政府機関
学術・研究機関
病院・医療機関
コンサルティング・サービス企業
地域別
北米
米国
カナダ
ヨーロッパ
ドイツ
英国
フランス
イタリア
その他のヨーロッパ
アジア太平洋
日本
中国
インド
その他のアジア太平洋地域
ラテンアメリカ
中東・アフリカ
GCC諸国
中東・アフリカ
2023年7月、シグナントヘルスはDSGを買収し、包括的なEDC/DDC機能を含む製品スイートを拡張し、市場での地位をさらに強化した。
2022年10月、オラクルはObvioHealthと協業し、eConsent、eCOA、ePRO機能を含むObvioHealthのDCTプラットフォームとモバイルアプリ、ObvioGoをOracle Clinical One Cloud Service(Clinical One)にシームレスに統合できるようにした。
2023年10月、クラリオはTrial Dataと提携し、彼らの豊富なDCT経験とeCOAソリューション、中国における臨床試験業務の深い経験を組み合わせることで、中国で臨床試験をサポートするスポンサーの臨床試験戦略の能力と柔軟性を向上させました。
【目次】
1 はじめに (ページ – 58)
1.1 調査目的
1.2 市場の定義
1.2.1 包含と除外
1.3 市場範囲
1.3.1 市場セグメンテーション
図1 電子転帰評価(ECOA)ソリューション市場のセグメンテーション
1.3.2 地域範囲
1.4 考慮した年
1.4.1 通貨
表1 米ドルへの換算に使用した為替レート
1.5 利害関係者
1.6 景気後退の影響
2 調査方法 (ページ – 63)
2.1 調査データ
図2 調査デザイン
2.2 二次資料
2.2.1 二次資料からの主要データ
2.3 一次データ
2.3.1 一次資料
2.3.1.1 一次資料からの主要データ
2.3.1.2 主要な業界インサイト
2.3.2 一次インタビューの内訳
図3 一次インタビューの内訳: カテゴリー別、呼称別、地域別
2.4 調査手法の設計
図4 調査手法:仮説構築
2.5 市場規模の推定
図5 供給側市場の推定:収益シェア分析
2.5.1 ボトムアップアプローチ
図6 電子転帰評価(エコア)ソリューション市場:ボトムアップアプローチ
図7 需要側アプローチ:電子転帰評価(ecoa)ソリューションに対するエンドユーザーの支出
2.5.2 トップダウンアプローチ
図8 電子転帰評価(ecoa)ソリューション市場:トップダウンアプローチ
表 2 因子分析
図9 電子転帰評価(エコア)ソリューション市場:促進要因、阻害要因、機会、課題の分析によるCAGR予測
図 10 CAGR予測: 供給サイド分析
2.6 市場の内訳とデータ三角測量
図11 データ三角測量の方法
2.7 前提条件
2.7.1 市場規模の仮定
2.7.2 調査全体の前提
2.8 制限事項
2.8.1 範囲に関する限界
2.8.2 方法論に関する限界
2.9 リスク評価
表3 電子転帰評価(エコア)ソリューション市場:リスク評価
2.1 電子転帰評価(エコア)ソリューション市場:景気後退の影響分析
表4 世界のインフレ率予測、2021~2028年(成長率)
表5 米国の医療費支出、2019年~2022年(百万米ドル)
表6 米国の医療費支出、2023~2030年(百万米ドル)
3 要約(ページ数 – 81)
図12 電子転帰評価(エコア)ソリューション市場、コンポーネント別、2024年対2029年(百万米ドル)
図13 ウェアラブル、モバイル機器、その他の機器の電子臨床転帰評価(エコア)ソリューション市場:モデル別、2024年対2029年(百万米ドル)
図14 電子転帰評価(エコア)ソリューション市場、製品別、2024年対2029年(百万米ドル)
図 15 電子転帰評価(エコア)ソリューション市場:展開モデル別、2024 vs. 2029年(百万米ドル)
図 16 電子転帰評価(エコア)ソリューション市場:用途別、2024 年対 2029 年(百万米ドル)
図17 臨床試験向け電子転帰評価(エコア)ソリューション市場:治療分野別、2024年対2029年(百万米ドル)
図18 臨床転帰評価(エコア)ソリューション市場:エンドユーザー別、2024年対2029年(百万米ドル)
図19 電子転帰評価(ECOA)ソリューション市場:地理的スナップショット
4 プレミアムインサイト(ページ数 – 88)
4.1 電子転帰評価(エコア)ソリューション市場の概要
図20 政府のイニシアティブと研究開発費の急増が市場成長を牽引
4.2 アジア太平洋地域:電子転帰評価(ECOA)ソリューション市場:製品別、国別(2023年)
図21 2023年にアジア太平洋市場で最大のシェアを占めた日本
4.3 電子転帰評価(エコア)ソリューション市場:地理的成長機会
図 22 中国は予測期間中に最も高い成長率を記録する
4.4 電子転帰評価(エコア)ソリューション市場:地域ミックス(2021~2029年)
図23 北米が予測期間中も電子転帰評価(エコア)ソリューション市場を支配し続ける
4.5 臨床転帰評価(ECOA)ソリューション市場:先進国vs. 新興国
図 24 新興国は予測期間中に高い成長率を記録する
5 市場概要(ページ数 – 93)
5.1 はじめに
5.2 市場ダイナミクス
図25 電子臨床アウトカム評価(ECOA)ソリューション市場:促進要因、阻害要因、機会、課題
5.2.1 市場ダイナミクス:影響分析
5.2.2 推進要因
5.2.2.1 医療技術企業や製薬・バイオテクノロジー企業による製品開発のための研究開発費の増加
図 26 世界の医薬品研究開発費の増加(2014 年~2028 年
5.2.2.2 臨床研究に関連する運営コストと規制要件の上昇
5.2.2.3 政府による臨床試験への支援と資金提供
5.2.2.4 慢性疾患の蔓延とそれに伴う臨床試験の増加
5.2.2.5 臨床データの効率的なモニタリング
5.2.2.6 臨床試験全体のコストとスケジュールの削減
5.2.3 阻害要因
5.2.3.1 eCOAソリューションを開発・運用する熟練した専門家の不足
5.2.3.2 高い導入コストとメンテナンスコスト
5.2.3.3 eCOAソリューションに対するエンドユーザーの認識不足
5.2.4 機会
5.2.4.1 新興国における臨床試験の増加によるeCOA導入の急増
5.2.4.2 CROへの臨床試験プロセスのアウトソーシングの増加
5.2.4.3 手動データ解釈からリアルタイムデータ解析への段階的シフト
5.2.4.4 医療業界におけるモバイル技術の浸透の高まり
5.2.5 課題
5.2.5.1 進化する規制環境とコンプライアンス要件
5.2.5.2 データのセキュリティとプライバシーに関する懸念
5.2.5.3 相互運用性と統合性の欠如
5.2.5.4 従来の医療従事者からの抵抗とソフトウェアの信頼性に関する懸念
6 業界洞察 (ページ – 106)
6.1 はじめに
6.2 主要業界動向の概要
6.2.1 分散型臨床試験の増加
6.2.2 リアルワールドデータ(RWD)への注目の高まり
6.3 価値/サプライチェーン分析
図27 電子臨床アウトカム評価(ECOA)ソリューション市場:バリューチェーン分析(2023年)
6.4 エコシステム分析
図28 電子的臨床転帰評価(エコア)ソリューション市場:エコシステム分析(2023年)
6.5 技術分析
6.5.1 主要技術
6.5.1.1 機械学習
6.5.1.2 人工知能
6.5.1.3 モノのインターネット
6.5.1.4 統合API
6.5.2 補足技術
6.5.2.1 インタラクティブ・ボイス・レスポンス(IVR)
6.5.2.2 データ分析
6.5.2.3 遠隔医療
6.5.3 隣接技術
6.5.3.1 クラウドコンピューティング
6.5.3.2 ブロックチェーン
6.6 規制の状況
6.6.1 規制分析
6.6.1.1 北米
6.6.1.2 欧州
6.6.1.3 アジア太平洋
6.6.1.4 ラテンアメリカ
6.6.1.5 中東・アフリカ
6.6.2 規制機関、政府機関、その他の組織
表7 北米:規制機関、政府機関、その他の組織
表8 欧州: 規制機関、政府機関、その他の組織
表9 アジア太平洋: 規制機関、政府機関、その他の団体
表10 その他の地域: 規制機関、政府機関、その他の組織
6.7 ポーターの5つの力分析
表11 電子臨床アウトカム評価(エコア)ソリューション市場:ポーターの5つの力分析
6.7.1 競争上のライバル
6.7.2 買い手の交渉力
6.7.3 供給者の交渉力
6.7.4 代替品の脅威
6.7.5 新規参入の脅威
6.8 価格分析
6.8.1 平均販売価格動向(地域別
6.8.2 指標価格分析(製品別
表 12 電子転帰評価(Ecoa)ソリューションの平均販売価格(ソリューションタイプ別)(2023 年
6.9 ケーススタディ分析
6.9.1 事例1: 大手学術医療センターがメディデータの ecoa で新規診断骨髄腫患者をモニタリング
6.9.2 事例2: シグナントのスケール管理の専門知識により、関節症性乾癬試験のエンドポイントの正確性と信頼性が向上
6.10 特許分析
図 29 電子転帰評価(ecoa)ソリューションの上位特許所有者及び出願者(2011 年 1 月~2024 年 1 月)
図 30 電子転帰評価(エコア)ソリューション市場:特許分析(2011 年 1 月~2024 年 1 月)
図31 電子転帰評価(ecoa)ソリューション特許の上位出願国/地域(2011年1月~2024年1月)
表 13 電子転帰評価(エコア)ソリューション市場における特許/特許出願リスト(2021~2023 年
6.11 主要会議・イベント(2023~2024年
表14 電子転帰評価(エコア)ソリューション市場:会議・イベント詳細リスト
6.12 顧客のビジネスに影響を与えるトレンド/混乱
図 32 電子転帰評価(ECOA)ソリューション市場における収益シフト
6.13 主要ステークホルダーと購買基準
6.13.1 購入プロセスにおける主要ステークホルダー
図 33 上位 3 エンドユーザーの購買プロセスにおける利害関係者の影響力
表 15 上位 3 エンドユーザーの購買プロセスにおける利害関係者の影響力
6.13.2 購入基準
図34 エンドユーザーの主な購買基準
表16 エンドユーザーの主な購買基準
6.14 エンドユーザー分析
6.14.1 満たされていないニーズ
表17 電子転帰評価(エコア)ソリューション市場における満たされていないニーズ
6.14.2 エンドユーザーの期待
表18 電子転帰評価(エコア)ソリューション市場におけるエンドユーザーの期待
6.15 収益モデル分析
6.15.1 サブスクリプションモデル
6.15.2 ペイ・パー・スタディ・モデル
6.15.3 カスタマイズ・ソリューション・モデル
6.15.4 Saas(ソフトウェア・アズ・ア・サービス)モデル
6.15.5 コンサルティング&統合サービスモデル
6.16 投資の展望
図 35 電子転帰評価(エコア)ソリューション市場における最近の投資
…
【本レポートのお問い合わせ先】
www.marketreport.jp/contact
レポートコード:HIT 8947